В основе устройств Эфферон® лежит передовая технология, разработанная российскими учёными, защищённая международными патентами [1]
Что было раньше?
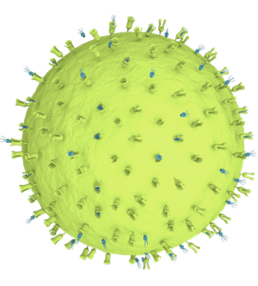
ЛПС-селективные сорбенты не
обладают порами требуемого объёма
и морфологии для эффективного
удаления избытка цитокинов и других
экзо- и эндогенных токсинов.
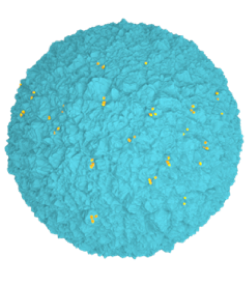
Пористая структура неселективных сорбентов не позволяет эффективно удалять ассоциаты и мицеллы липополисахаридов из цельной
крови.
В чём новизна технологии
Эфферон ЛПС?
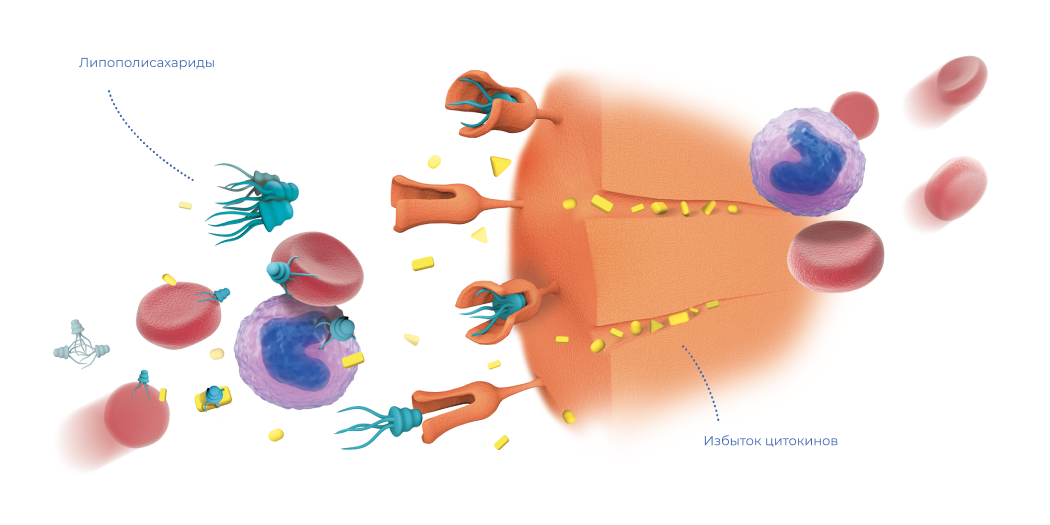
Первый компонент
сорбента — матрица из сверхсшитого полистирола
Полимеры такого строения были впервые получены и описаны Даванковым и Цюрупой [3-4]. Их отличительными особенностями являются недостижимая для других органических полимерных материалов степень пористости (удельная поверность 700-900 м2/г) и структурно обусловленная низкая тромбогенность. Крупные замкнутые полости в их объёме могут достигать диаметра до 100 нм, а пронизывающие матрицу каналы существенно меньше. Такое строение обеспечивает быстрый массоперенос малых и средних белков молекулярной массы 10-40 кДа (к которым относятся молекулы DAMP, Ил-6, Ил-1б и другие цитокины) и предотвращает потерю более крупных белков, таких как альбумин (66 кДа).
Адсорбция цитокинов в порах протекает по неспецифичному механизму (гидрофобные и ван дер Ваальсовы взаимодействия) и является обратимым равновесным процессом. В результате степень удаления оказывается выше для белка, исходно присутствующего в более высокой концентрации [5]. Таким образом, в ходе гемоперфузии через подобные сорбенты клиренсы цитокинов снижаются во времени. Подобный механизм уместен для снижения пиковых концентраций этих важных медиаторов воспалительного процесса, при этом их уровни поддерживаются выше нулевых значений.

Микрофотография сорбента
Второй компонент сорбента — синтетический лиганд к домену Липид А молекулы ЛПС, ковалентно иммобилизованный на поверхности сверхсшитой полистирольной матрицы
Связывание лиганда с глюкозаминфосфатными остатками и гидрофобными ацильными заместителями молекулы ЛПС протекает по механизму, сходному со связыванием молекулы ЛПС с обогащённым остатками лизина Полимиксином Б [6].
Молекулярная масса мономерного ЛПС варьирует от 2,5 до 70 кДа и обычно принадлежит диапазону 10-20 кДа. Размеры соединений ЛПС с белками плазмы крови и катионами Ca2+ и Mg2+ достигают на порядки больших размеров, до 1 000 000 кДа [7].
Стратегии удаления ЛПС из крови, основанные на адсорбции в порах определённого диаметра, не способны снизить его концентрацию ниже терапевтически значимых уровней. Напротив, связывание молекулы ЛПС с аффинным лигандом является необратимым процессом. Стендовые эксперименты демонстрируют [8], что остаточная концентрация ЛПС в бычьей крови после перфузии через немодифицированный сверхсшитый полистирол снижается лишь до 0,3-0,5 ЕЭ/мл (такие высокие уровни ассоциируются с выраженной эндотоксемией), в то время как модицифированный ЛПС-связывающим лигандом сорбент снижает концентрацию ЛПС ниже опасных значений (менее 0,05 ЕЭ/мл).

Что в результате?
1. Bessonov I.V., Morozov A.S., Kopitsyna M.N. // A polymeric sorbent, preparation and use thereof, patent No WO2018217137, 2018.
2. Magomedov M.A., Kim T.G., Masolitin S.V., Yaralian A.V., Kalinin E.Yu., Pisarev V.M. // Use of sorbent based on hypercrosslinked styrene-divinylbenzene copolymer with immobilized LPS-selective ligand In hemoperfusion for treatment of patients with septic shock. General Reanimatology. 2020;16(6):31-53.
3. Davankov V.A., Rogozhin S.V., Tsjurupa M.P. // Macronet polystyrene structures for ionites and method of producing same, patent No US3729457A, 1973.
4. Davankov V.A., Tsyurupa M.P. // Structure and properties of hypercrosslinked polystyrene — the first representative of a new class of polymer networks. Reactive Polymers. 1990;13(1-2):27-42.
5. Honore P.M. et al. // Cytokine removal in human septic shock: Where are we and where are we going? Annals of intensive care. 2019;9(1):56.
6. David S.A. // Towards a rational development of anti‐endotoxin agents: novel approaches to sequestration of bacterial endotoxins with small molecules. Journal of Molecular Recognition. 2001;14(6):370-387.
7. Caroff M., Karibian D. // Structure of bacterial lipopolysaccharides. Carbohydrate Research. 2003;338(23):2431-2447.
8. Morozov A.S. et al. // A selective sorbent for removing bacterial endotoxins from blood. Russian Journal of Physical Chemistry A, 2016;90(12):2465-2470.




